Corrosie van roestvast staal in alkaliën en hypochloriet
Bijtende soda (NaOH), kaliloog (KOH) en gecalcineerde soda (Na2CO3) zijn ware alkalische chemicaliën. Technisch gesproken zijn hypochlorieten alkalische oxiderende zouten, maar ze vertonen een gedrag dat sterk verschilt van dat van alkaliën.
Door: A.J. Schornagel
Natriumhydroxide of bijtende soda is de meest gebruikte en beschikbare alkalische chemicalie. Het merendeel van het geproduceerde NaOH wordt geproduceerd als bijproduct van chloor via het gebruik van elektrolytische cellen. Deze cellen zijn van het diafragma-, kwik-, of membraan-type. Er wordt NaOH verhandeld zoals het wordt geproduceerd in genoemde cellen, maar het merendeel wordt verdampt en verkocht als 50 of 73% oplossingen of als kristalwatervrije korrels. De meeste uiteindelijke toepassingen van bijtende soda vereisen oplossingen van betrekkelijk lage concentratie. De tabellen 1 tot en met 5 geven het gedrag weer van onder andere roestvast staal. Tabel 3 is met name van toepassing op de corrosiviteit van bijtende soda uit diafragma- en kwikcellen. Geen bespreking van constructiemateriaal voor NaOH zou compleet zijn zonder de noodzaak van veiligheid in elke toepassing te benadrukken. Oplossingen van bijtende soda, zeker als ze warm zijn, zijn buitengewoon schadelijk voor het menselijk lichaam. Blootstelling kan onmiddellijke en hevige brandwonden veroorzaken, waarbij ogen bijzonder gevoelig zijn. Vaak moet bij materiaalselectie rekening worden gehouden met mogelijke blootstelling van personen, zodat er dikwijls moet worden gekozen voor een duurder maar betrouwbaarder materiaal.
Austenitisch roestvast staal, voornamelijk de typen 304 en 316, zijn zeer bestand tegen bijtende soda in concentraties tot 50% en temperaturen tot ongeveer 95°C (zie tabellen 1, 3, 4, 5 en 6).

Tabel 1 Corrosie van metalen en legeringen in NaOH bij verschillende concentraties (laboratoriumproeven bij kamertemperatuur).

Tabel 2 Corrosie van metalen en legeringen in 30 – 50% NaOH.
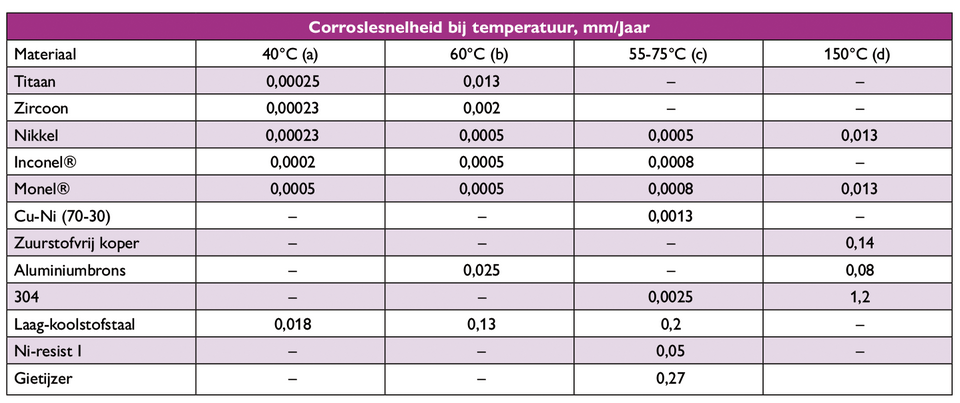
Tabel 3. Corrosie van metalen en legeringen in 50% NaOH bij verschillende temperaturen.
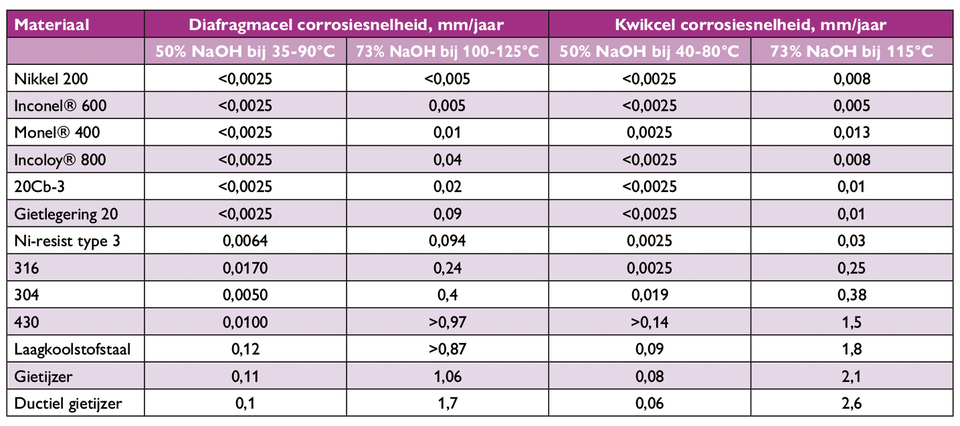
Tabel 4. Vergelijking van corrosiviteit van NaOH gefabriceerd in diafragmacellen en kwikcellen.
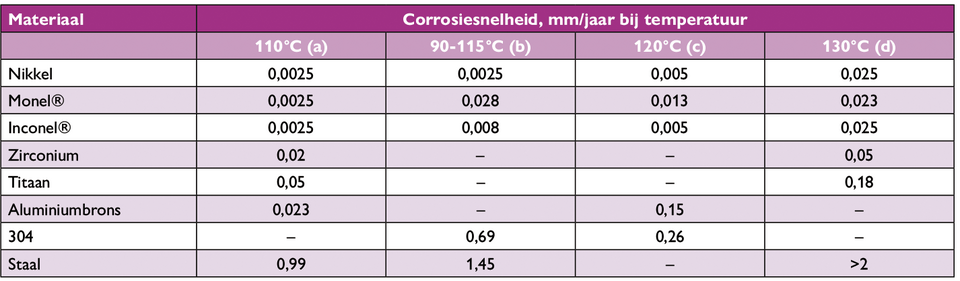
Tabel 5. Corrosie van metalen en legeringen in 70 - 73% NaOH bij verschillende temperaturen.

Tabel 6. Corrosie van metalen en legeringen in het NaOH-fusieproces.
Afbeelding 1 toont de corrosiesnelheden en een spanningscorrosiegrens voor austenitisch roestvast staal dat is blootgesteld aan NaOH-oplossingen. Er wordt geen onderscheid gemaakt tussen de typen 304 en 316, omdat hun gedrag zo sterk overeenkomt. Van belang is de spanningscorrosie zone, die berust op bekende schadegevallen en die een aanwijzing vormt voor potentiële scheuringsproblemen boven ongeveer 105°C. Er wordt algemeen aangenomen dat deze vorm van scheurvormende spanningscorrosie in bijtende soda optreedt zonder onderscheid te maken tussen de diverse austenitische RVS-typen. De scheuring wordt beïnvloed door het spanningsniveau en de temperatuur. Om een bepaalde mate van zekerheid te geven wordt als maximum bedrijfstemperatuur 95°C aanbevolen. Er is scheurvormende spanningscorrosie waargenomen op microscopische schaal bij laboratoriumproeven bij concentraties van 10% bij een temperatuur van 100°C.

Hoewel austenitisch roestvast staal makkelijk scheurt in neutrale en zure chloriden boven 60°C, schijnt het effect van chloriden in een alkalische oplossing nihil te zijn. Zolang de oplossing alkalisch blijft, verloopt de scheurvormende spanningscorrosie volgens die van loogbrosheid en blijft zich alleen voordoen in het gebied zoals aangegeven op afbeelding 1. Een oplossing van 0,5 g/l NaOH met een pH 12 is voldoende alkalisch. De bezorgdheid om verontreiniging van bijtende soda met chloriden bij gebruik van apparatuur gemaakt van roestvast staal berust eigenlijk nergens op. Meer zorg baren invloeden van buitenaf. Schade als gevolg van uitwendige blootstelling, gebrekkige isolaties, verontreinigd water en onjuiste schoonmaak- en opslagmethodes veroorzaken meer problemen dan het verwerken van bijtende soda. Omdat putcorrosie onder inwerking van chloriden en/of scheurvormende spanningscorrosie vaak van primaire zorg zijn, dient bij materiaalselectie het relatieve gedrag op dit terrein in ogenschouw te worden genomen. Hoewel de typen 304 en 316 vergelijkbaar gedrag vertonen in bijtende soda en bij standaard spanningscorrosieproeven, vertoont 316 een beter totaal gedrag vanwege zijn weerstand tegen putcorrosie (de rol van in de alkalische oplossingen opgeloste zuurstof kan in dit opzicht significant zijn).
Verder presteren de laag-koolstofhoudende typen net iets beter vanwege hun weerstand tegen sensitisering. Dit zou erop kunnen duiden dat, tenzij de nodige controlemogelijkheden om eventuele corrosie in een vroegtijdig stadium op te sporen aanwezig zijn, er gebruik moet worden gemaakt van type 316L (een molybdeenhoudend, laag-koolstoftype 316). Toepassingen van roestvast staal voor gebruik met bijtende soda omvatten leidingwerk, afsluiters, pompen en apparaten. Toepassing voor transportleidingen komt veel voor. Er doen zich zelden moeilijkheden voor met oplossingen met concentraties tussen 10 en 20%, omdat verstopping en stilstand slechts sporadisch voorkomen. Een ander mogelijk risico vormt de toetreding van kwik als een verontreiniging in bijtende soda gewonnen uit kwikcellen. Dit kan bijdragen tot scheuring of putvorming in austenitisch roestvast staal bij kwikconcentraties van slechts enkele ppm. Er doen zich ook gevallen voor waarbij roestvast staal niet kan worden gebruikt vanwege het gevaar dat er Cr6+-ionen in de kwikcel terecht kunnen komen.
Pompen en afsluiters, gemaakt van roestvast gietstaal, gedragen zich zeer bevredigend in bijtende soda. De aard van de gegoten oppervlakken beperkt scheurvormende spanningscorrosieproblemen tot een minimum en gietwerk is in het algemeen aanvaardbaar in situaties die de capaciteiten van smeedwerk verre te boven gaan. De corrosiesnelheden van gietwerk zijn ongeveer vergelijkbaar met die van smeedwerk. Een andere praktische toepassing van roestvast staal in bijtende soda is bij verdampingsprocessen, waarbij warmte-wisselaarpijpen van hoogzuiver 26-1 (een laag-koolstofhoudende versie van 446, die niobium en molybdeen bevat) worden gebruikt. Sommige hoge temperatuurtoepassingen bleken effectief te werken daar waar de corrosie van nikkel excessief was. Dit is waarschijnlijk het gevolg van de aanwezigheid van hypochloriet- of chloraatverontreinigingen. Het debat aangaande nikkel versus ferro-legeringen gaat nog wel even door, maar beide metalen vertonen bevredigende prestaties. De legering 26-1 is bruikbaar tot 175°C, afhankelijk van de concentraties bijtende soda, chloride en verontreinigingen. Als 26-1 wordt aangetast, dan schijnt er doorgaans sprake te zijn van interkristallijne scheuring.
Kaliumhydroxide
Kaliumhydroxide, ook wel bekend als kaliloog, heeft een hoger kookpunt dan NaOH bij gelijke concentraties. Het wordt zelden verdampt boven een concentratiewaarde van 90%. Het komt in corrosiegedrag en veiligheidsvereisten sterk overeen met NaOH. Corrosie en degradatie van materiaal is hetzelfde in KOH als in NaOH. Er bestaan aanwijzingen dat KOH iets agressiever is dan NaOH, maar dit is meer gerelateerd aan het hogere kookpunt en blootstelling aan naar alle waarschijnlijkheid hogere temperaturen.
Natriumcarbonaat of gecalcineerde soda
Gecalcineerde soda is een alkalisch zout. Het wordt veel gebruikt bij alkalische processen om Na2O te leveren. In oplossing veroorzaakt Na2CO3 minder alkaliniteit dan het hydroxide. Een 0,1% oplossing geeft een pH 11, terwijl een volledig verzadigde oplossing 35% bedraagt met een pH 12,5. De gerelateerde bicarbonaten (natriumbicarbonaat en NaHCO3) zijn minder alkalisch, maar ze zullen overgaan in carbonaten bij hoge temperatuur en verhogen daarmee de pH van de oplossing. De veiligheidseisen voor Na2CO3 zijn wat minder stringent vanwege de lagere alkaliteit. Gecalcineerde soda kan makkelijk worden verwerkt met alles wat ook geschikt is voor bijtende soda. Net als bij andere alkalische oplossingen, verschaft de aanwezigheid van carbonaationen (CO2-3) gewoonlijk een inhibiterend effect op metalen. Als nulcorrosie nodig wordt geacht, dan voldoet roestvast staal zeer goed. Roestvast staal heeft een spanningscorrosiegebied dat gelijk is aan die bij bijtende soda, maar wel bij aanzienlijk lagere temperaturen.
Hypochlorieten
Hypochlorieten Deze alkalische oxiderende zouten behoren tot de corrosiefste zouten. Natriumhypochloriet (NaOCl), wordt geproduceerd als een vloeistof door 20% NaOH te chloreren. Resulterende sodableekoplossingen bevatten ongeveer 15% NaOCl, met wat rest NaOH ter bevordering van de stabiliteit. Deze industriële bleekmiddelen worden verdund tot concentraties van ongeveer 5% voor huishoudelijk gebruik. Om de stabiliteit nog verder te verbeteren, mag de gebruikte NaOH geen zware metalen bevatten en het NaOCl moet worden opgeslagen in donkere of in polyethyleen flessen bij temperaturen onder 30°C. Natriumhypochloriet bestaat niet als een stabiele vaste stof. De vaste hypochlorieten omvatten lithium-, calcium-, strontium- en bariumhypochloriet, hoewel de enige belangrijke toepassingen zijn weggelegd voor calcium-hypochloriet (Ca(OCl)2). Vast Ca(OCl)2 valt snel uiteen bij hoge temperatuur (175°C), waarbij chloor vrijkomt. Het reageert ook heftig met veel oxideerbare organische verbindingen. Oplossingen van calciumhypochloriet komt men tegen bij bleken, ontsmetten of het wegnemen van geuren. Het vaste product wordt vaak opgelost in water waarbij verdunde oplossingen worden gemaakt voor bleken en waterzuivering.
Natriumhypochloriet
Natriumhypochloriet Het hypochlorietion (OCl-) komt wat zijn werking op materiaal overeen met nat chloorgas. Slechts weinig metalen vertonen goede weerstand, zelfs bij lage temperatuur en concentraties. Omdat hypochlorietoplossingen instabiel zijn bij neutrale en lage pH, bevatten ze vaak overschot alkali, dat de agressiviteit wat beperkt. Hooggelegeerd ijzer-chroom-nikkel, zoals 20Cb-3, is wel gebruikt in het bijzonder voor pompmateriaal, in wat minder agressieve milieus. Natriumhypochloriet wordt gewoonlijk bewaard bij lage temperatuur om uiteenvallen te voorkomen. De invloed van hogere temperatuur, zelfs in de verdunde oplossingen, vindt zijn weerslag in de corrosiesnelheden (tabel 8). De aanwezigheid van ionen van zware metalen, vooral in het geval van hogere oplossingsconcentraties, veroorzaakt vaak instabiliteit die gepaard gaat met decompositie. Deze neiging sluit metalen uit die anders wel bruikbaar zouden zijn, omdat uiteenvallen vaak een corrosiereactie in gang zet. Sommige van de nieuwere super RVS-typen tonen bruikbare weerstand in bepaalde NaOCl-oplossingen. Er is in dit verband melding gemaakt van succesvol gebruik van een hooggelegeerde duplexlegering (Ferralium 255) in een NaOCl-wasser. Als roestvast staal wordt aangetast door NaOCl, dan vindt dat doorgaans plaats in de vorm van put- en/of spleetcorrosie. Calciumhypochloriet Hoewel geproduceerd als vaste stof, komen de reacties van Ca(OCl)2 in oplossing overeen met die van NaOCl. De aanbevolen temperatuursniveaus voor Ca(OCl)2 liggen iets hoger, waarschijnlijk vanwege hun decompositietemperatuur. Net als NaOCl, is het calciumhypochloriet onstabiel bij lagere pH, maar het kan sterker worden geconcentreerd. Tabel 9 geeft corrosiesnelheden voor 316 en enige andere metalen.
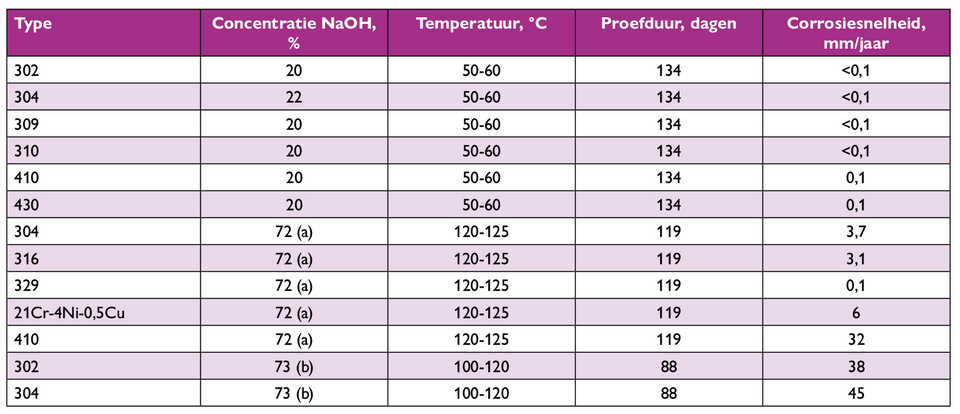
Tabel 7. Corrosie van roestvast staal in NaOH-oplossingen.

Tabel 8. Corrosie van metalen en legeringen in NaOCl oplossingen bij verhoogde temperaturen.

Tabel 9. Corrosie van metalen en legeringen in Ca(OCl)2.
(Note van de redactie: Zeer veel dank is wederom verschuldigd aan Christine van der Ven voor het optimaliseren en het leesbaar maken van de tabellen!)



