Elektrochemische NDO-methode voor bepaling gevoeligheid van austenitisch roestvast staal voor ic
Gevoeligheid voor interkristallijne corrosie van austenitisch roestvast staal kan zich voordoen na bepaalde behandelingen, bijvoorbeeld als gevolg van lasbewerkingen of gloeien. Hoewel van te voren in het laboratorium kan worden vastgesteld of een bepaalde staalsoort al of niet gevoelig is, is het toch van grote waarde over de mogelijkheid te beschikken om ter plaatse en zonder beschadiging van de constructie na te gaan of het materiaal door een bepaalde bewerking toch gevoelig is geworden voor interkristallijne corrosie.
A.J. Schornagel
Inleiding
Voor de bepaling van de gevoeligheid van roestvast staal en gerelateerde legeringen voor interkristallijne corrosie, wordt vaak gebruik gemaakt van dompelproeven in het laboratorium. Het gaat hierbij dan meestal om dompelproeven in kokende oplossingen van zwavelzuur, waaraan kopersulfaat is toegevoegd, of salpeterzuuroplossingen (bijvoorbeeld de Strauss-Hadfield-test en de Huey-test) en er wordt ook wel gebruik gemaakt van etsproeven in oxaalzuur (Streichertest).
De proeven in kokende oplossingen hebben drie grote nadelen:
- ze zijn destructief (voor de proef moeten monsters worden uitgenomen);
- ze zijn niet snel genoeg;
- het is lastig om de mate van sensitisering te kwantificeren.
Deze dompelproeven worden gekenmerkt door een hogere gevoeligheid naarmate het te beproeven staal sterker is gesensitiseerd, maar voor het vaststellen van geringe mate van sensitisering zijn ze niet gevoelig genoeg.
De etsproef in oxaalzuur is vrij snel en kan niet-destructief zijn, maar de mate van sensitisering is moeilijk te bepalen en metallografische voorbehandeling is noodzakelijk. Met betrekking tot het in oplossing gaan van bepaalde fasen van de microstructuur van roestvast staal, met name carbiden, zijn er geschikte proefomstandigheden geschapen op basis van het principe van reactivering vanuit de passieve en! of transpassieve toestand [1], waarmee het mogelijk is om het verloop van interkristallijne corrosie te volgen.
Enkel en dubbellus EPR
De enkel en dubbellus elektrochemische potenriokinetische reactiveringstechnieken (SL-EPR en DL-EPR) zijn technieken die gebruik maken van potentiodynamische metingen waarmee het mogelijk is om de mate van gevoeligheid voor sensitisering van austenitisch roestvast staal vast te stellen. De proeven worden uitgevoerd met een standaard elektrolytoplossing van 0,5 M H2SO 4 + 0,01 M KSCN bij kamertemperatuur. Bij de SL-methode (zie afbeelding 1 ), krijgt het monster eerst de gelegenheid om te stabiliseren in de oplossing, waarbij het een open potentiaalwaarde aanneemt die doorgaans rond de -400 m V SCE ligt (punt 2 op afbeelding 1).
Nadat het monster voldoende is gestabiliseerd, wordt er een potentiaal van +200 mVSCE aangelegd om het staal in de passieve toestand te brengen (punt 1 op afbeelding 1).
Vervolgens wordt de potentiaal verlaagd tot de eerdere open potentiaal (punt 2).
Als de potentiaal wordt verlaagd zullen de korrelgrenzen in geval van sensitisering als eersten actief worden. Dus zal de totale anodische stroom (of lading Q) die passeert als de potentiaal met een vaste snelheid afneemt evenredig zijn met de grootte van het geactiveerde korrelgrensoppervlak en is dus een indicatie voor de mate van sensitisering.
De DL- methode komt op tal van punten overeen met de SL-methode (zie afbeelding 2). Wederom krijgt het monster de gelegenheid om te stabiliseren bij een open potentiaal (punt 1 op afbeelding 2). Vervolgens wordt, in plaats van potentiostatisch passiveren, de potentiaal potenriodynamisch opgevoerd van de open potentiaal, dus vanaf circa -400 mVSCE' tot +300 mVSCE (punt 2 op afbeelding 2), waarna weer terug wordt gegaan naar de oorspronkelijke open potentiaal. Op dat punt wordt de piekstroom van de anodische neus van de eerste polarisatie (Ia) vergeleken met de piekstroom van de teruggaande polarisatie (Ir) Van de stroom bij teruggang wordt aangenomen dat deze voornamelijk het gevolg is van het reactiveren van de chroomverarmde korrelgrenzen. De verhouding Ir/Ia wordt gebruikt om de mate van sensitisering te bepalen.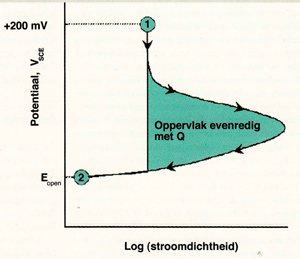
Afbeelding 1 Principe van SL-EPR meting.
Afbeelding 2 Principe van DL-EPR meting.
Niet destructief EPR-onderzoek
Voor het EPR-onderzoek wordt in de regel gebruik gemaakt van monsters die uit bestaande onderdelen worden genomen. De test is dus destructief. Om er een niet-destructieve test van te maken zou het mogelijk moeten zijn om de proefopstelling zodanig aan te passen dat de meting op een bestaande constructie kan worden uitgevoerd. Dit betekent dus dat de elektrochemische cel en de bijbehorende elektrodes in een apparaat met een handzaam formaat worden ondergebracht.
In het verleden is er wel geëxperimenteerd met in situ metingen waarbij gebruik werd gemaakt van meetcellen van diverse pluimage, zoals een roestvaststalen buisje dat aan een zijde was afgesloten met een poreuze prop, die was doordrenkt met elektrolytoplossing en waarbij het staal van de buis als tegenelektrode fungeerde. Er werd dan via een zoutbrug of via een brug gevuld met agar-agar-verbinding gemaakt met de referentie elektrode. Hoewel dergelijke meetopstellingen vaak in vergelijk met metingen in het laboratorium verbluffend goede resultaten gaven, werden ze toch niet geaccepteerd, omdat ze niet waren beschreven in normen, zoals bijvoorbeeld van ASTM. Toch worden er steeds opnieuw pogingen ondernomen om ook te velde metingen te kunnen uitvoeren.
Gelvormige elektrolyt
De eerste stap naar in situ meten bestaat uit het vinden van een geschikte vervanger van de elektrolytoplossing. Toepassing van een gelvormige elektrolyt voor corrosieonderzoek is al jaren lang bekend. Zo werd er bijvoorbeeld gebruik gemaakt van gel-elektrolyt voor een corrosieonderzoek aan verschillende soorten staaldraad [2].
In referentie [3] werd er gebruik gemaakt van de aerosol A-380 siliciumdio;jde gel waaraan H2S04 en KSCN zijn toegevoegd. De kleine en handige elektrochemische corrosiecel was gemaakt van een injectiespuit. Er bleek een goede correlatie te bestaan tussen de resultaten, behaald met de gel-elektrolyt en een standaard-laberatoriummethode.
Het gebruik van gel-elektrolyt heeft de volgende voordelen in vergelijking met vloeibare elektrolyt:
- betere simulatie van corrosieprocessen in vaste media, zoals staal, beton, voedingswaren;
- de mogelijkheid tot analyse van de corrosieproducten die in de gel kunnen worden vastgehouden;
- geen noodzaak voor het gebruik van een speciale corrosiecel en afdichtingen zoals nodig zijn voor een vloeibare oplossing;
- de mogelijkheid tot het doen van elektrochemische corrosiemetingen aan onregelmatige oppervlakken, zoals lassen.
Nadelen zijn van de gel-elektrolyt zijn:
- bereiding van de gel (hechtingseigenschappen, viscositeit) is moeilijker dan de bereiding van een vloeibare elektrolyt;
- de stabiliteit is op langere termijn moeilijk te handhaven;
- de gel kan de corrosiemechanismen beïnvloeden, omdat de in de gel aanwezige chemicaliën kunnen optreden als katalysator of als inhibitor.
Correlatie tussen gelvormige en vloeibare elektrolyt
Cihal, Blahetová en Lasek [5] hebben onderzocht of er voldoende correlatie bestond tussen EPR-metingen met gelvormige elektrolyt voor in situ metingen en EPR-metingen met vloeibare elektrolyt, zoals die in het laboratorium worden uitgevoerd. De te onderzoeken gelaste metaalmonsters zijn nat geschuurd met SiC-papier met de gradaties 60 tot 1200, waarna werd ontvet en gespoeld met gedistilleerd water en gedroogd met lucht. De te onderzoeken oppervlakken werden afgeplakt met plakband waarin gaten (∆ 3 mm) waren aangebracht op afstanden van 1, 2, 3, ... 9 mm tussen de as van de las en de middelpunten van de gaten in het plakband.
Meetmilieu en opstelling
De elektrochemische potentiokinetische reactiveringsmeringen zijn uitgevoerd volgens ISO TC 156/WG9 - EPR
Double Loop Test (Method B) [1]. De meting liep van een aanvangspotentiaal van -700 mV tot +500 mV en weer terug naar -700 mVmeteen constante polarisatiesnelheid van 1,67 m V/s. Alle potentialen zijn weergegeven ten opzichte van de verzadigde calomelelektrode (SCE).
De elektrochemische metingen zijn uitgevoerd met een waterige oplossing van 2,0 mol/I H2SO4 + 0,01 mol/I
KSCN. De gel-elektrolyt werd bereid door waterglas te mengen met 2,0 mol/I H2SO4 + 0,01 mol/I KSCN. Parallel met de EPR-test in gel en in een vloeibare elektrolytoplossing, bestaande uit eveneens 2,0 mol/I H2SO4 + 0,01 mol/I KSCN, beide bij kamertemperatuur, werden er ook standaard kookproeven uitgevoerd in waterige oplossingen van 50% H2SO4 + 40 g/l Fe2(SO4)3.9H2O respectievelijk 10% H2SO4 + 130 g/l CuSO4.5H2O.
Er werd gemeten aan een aantal roestvast-staaltypen, waaronder 904L, 304L (1.4306), beide laagkoolstofhoudend (C-gehalte respectievelijk 0,02% en 0,025%).
Voor het bepalen van veranderingen in gevoeligheid van verschillende delen van de lasverbinding (bijvoorbeeld op verschillende afstanden van de las) werden er miniatuurcellen gemaakt van kleine injectiespuiten met een inhoud van 3 - 12 ml. Op de uitgang van de spuit werd een speciale cilinder geplaatst die was gemaakt van PTFE, waarin kleine gaatjes waren aangebracht met diameters van minder dan 3 mm ten behoeve van de elektrochemische verbinding tussen de werkelektrode, de referentie-elektrode en de tegenelektrode. Voor de verbinding tussen de referentie calomelektrode en de testoplossing werd een dubbele vloeistofbrug gebruikt. Technische details van de miniatuurcel zijn te vinden in [4].
Voordelen van het gebruik van de combinatie gelvormige elektrolyt en een miniatuurcel in de vorm van een injectiespuit voor het bepalen van de gevoeligheid van roestvast staal voor interkristallijne corrosie zijn:
- klein formaat van de opstelling zodat deze ook kan worden gebruikt op moeilijk toegankelijke plaatsen, zoals hoeklassen;
- lassimulatie op relatief kleine proefstukken in het laboratorium kan een microstructuur opleveren die afwijkt van die welke in de praktijk wordt aangetroffen bij grootschaliger werkstukken;
- de gel-elektrolyt kan worden aangebracht in de vorm van een klein druppeltje (oppervlak circa 1 x 5 mm) evenwijdig aan de lasrichting.
Resultaten
Afbeelding 3 toont het verloop van de verhouding Ir/Ia als functie van de afstand van het centrum van de las voor 904L. In de standaard testoplossing werden minimale reactiveringswaarden gemeten, hetgeen in de lijn der verwachtingen lag vanwege het hogere Mo- en Cr-gehalte van dit staaltype. Daarom is er ook gemeten in een wat agressiever milieu: er werd HCl aan de elektrolyt toegevoegd. Het resultaat was veelzeggend. Er werd geconstateerd dat voor het lassen gebruik was gemaakt van een onjuist elektrodetype, waardoor er legeringselementen verloren zijn gegaan als gevolg van verbranding. Een opvolgende dompelproef wees uit dat er verwaarloosbare interkristallijne aantasting plaatsvond in de warmtebeïnvloede zone en het basismetaal, maar dat een dendritisch gebied van de las en de fusiezone tussen lasmetaal en basismetaal verhoogde corrosiegevoeligheid te zien gaven die gepaard ging met sterke aantasting van dendrieten en korrelgrenzen.
Afbeelding 4 toont het verloop van de verhouding I/Ia als functie van de afstand van het centrum van de las voor 304L (1.4306). Bij dit staal trad er op een afstand van 6 mm van het centrum van de las een maximum op
in de Ir/Ia verhouding, hetgeen duidt op een ter plaatse maximale gevoeligheid voor interkristallijne corrosie.
Bij de dompelproef vertoonde het materiaal slechts een geringe mate van aantasting van de korrelgrenzen.
Afbeelding 3 DL-EPR meting aan 904L [5].
Afbeelding 4 DL-EPR meting aan 304L {5].
Conclusies
Het in situ meten van de gevoelig- Afstand van de as van de las, mm heid voor interkristallijne corrosie
met de DL-EPR methode van gelast of warmtebehandeld austenitisch roestvast staal met behulp van gel
vormige elektrolyt, geeft goede resultaten die tevens overeenstemmen met laboratoriummetingen, uitgevoerd met vloeibare elektrolyt.
Referenties
1. ISO TC 156/WG9: Corrosion of metals and alloys. Corrosion testing of Materials for Power Generation. Method for Electrochemical Potentiokinetic Reactivation Test (Based on CIHAL's Method), revised version 8, 1998.
2. D. Chambaere, F. Deruyck, J. Vanbrabant. Industrial application of an electrochemical corrosion test using a gel matrix as simulation for atmosferic and solid media. NV Bekaert SA.
3. Y. Kamenev, A. Nazarov, L. Kuusk, T. Maideburova. Proteetion of Metals, 1989, p. 833 - 837.
4. R. Fajkos. Electrochemical potentiokinetic polarization method for study of stainless steels properties. VSB Technical University, Ostrava.
5. V. Cihal, M. Blahetová, S. Lasek. Corrosion electrochemical testing in situ using a gel electrolyte. VSB Technical University, Ostrava.



